對(duì)乳腺腫瘤的認(rèn)識(shí)可追溯到公元前。公元前 460 年~ 前 377 年,古希臘著名醫(yī)生希波克拉底在其《文集》中對(duì)乳腺癌進(jìn)行了詳細(xì)描述,從而揭開(kāi)了人類認(rèn)識(shí)乳腺癌的歷史。
自從于公元1 世紀(jì),希臘 Leonides 醫(yī)生首先發(fā)現(xiàn)乳頭凹 陷是乳腺癌的一個(gè)重要體征,主張外科手術(shù)治療乳 腺癌,并首先實(shí)施了乳腺腫塊切除之后,乳腺癌的手術(shù)治療便正式拉開(kāi)了帷幕。
它先后經(jīng)歷了:
1、局限切除:僅切除腫塊或乳腺;
2、局部廣泛切除:切除范圍包括胸肌及周?chē)糠终5慕M織;
3、 乳腺癌根治術(shù)----整塊切除包括腫瘤在內(nèi)的全部乳腺、相當(dāng)范圍的乳腺皮膚和周?chē)M織,以及胸大、小肌和腋窩淋巴結(jié);(乳腺癌根治術(shù)的誕生,開(kāi)創(chuàng)了乳腺癌外科手術(shù) 史上的新紀(jì)元,使乳腺癌手術(shù)后局部復(fù)發(fā)率從 80% 降低到 20%左右,長(zhǎng)期生存率明顯提高,被譽(yù)為乳 腺癌手術(shù)的經(jīng)典術(shù)式。)
4、擴(kuò)大根治術(shù)階段:1949 年及 1951年,Margottini 和Urban 分別提出根治術(shù)合并胸膜 外和胸膜內(nèi)清除內(nèi)乳淋巴結(jié)的乳腺癌擴(kuò)大根治術(shù)。 1954年,Andreassen 和 Dahllverson 又在擴(kuò)大根治術(shù)的 基礎(chǔ)上加行鎖骨上淋巴結(jié)清掃。 1956 年,Arhelger 等 甚至還要行縱隔淋巴結(jié)清掃,分別稱之為超根治與擴(kuò)大超根治術(shù)。 從而把乳腺癌的外科手術(shù)治療推向 “超根治切除”的時(shí)代。
5、改良根治術(shù):保留胸大、小肌的根治術(shù);
6、保乳手術(shù)。
乳腺癌的手術(shù)治療經(jīng)歷了由小到大,再由大到小的輪回。是在影像、放療、化療、內(nèi)分泌治療、靶向治療等多學(xué)科診斷、治療手段發(fā)展的基礎(chǔ)上學(xué)科發(fā)展的必然結(jié)果和規(guī)律。
手術(shù)完成后不等于治療的結(jié)束,根據(jù)不同的腫瘤分期,分子分型還需進(jìn)行化療、放療、內(nèi)分泌治療,靶向治療等。以下是手術(shù)后各種治療選擇的標(biāo)準(zhǔn)。
乳腺癌復(fù)發(fā)風(fēng)險(xiǎn)分組
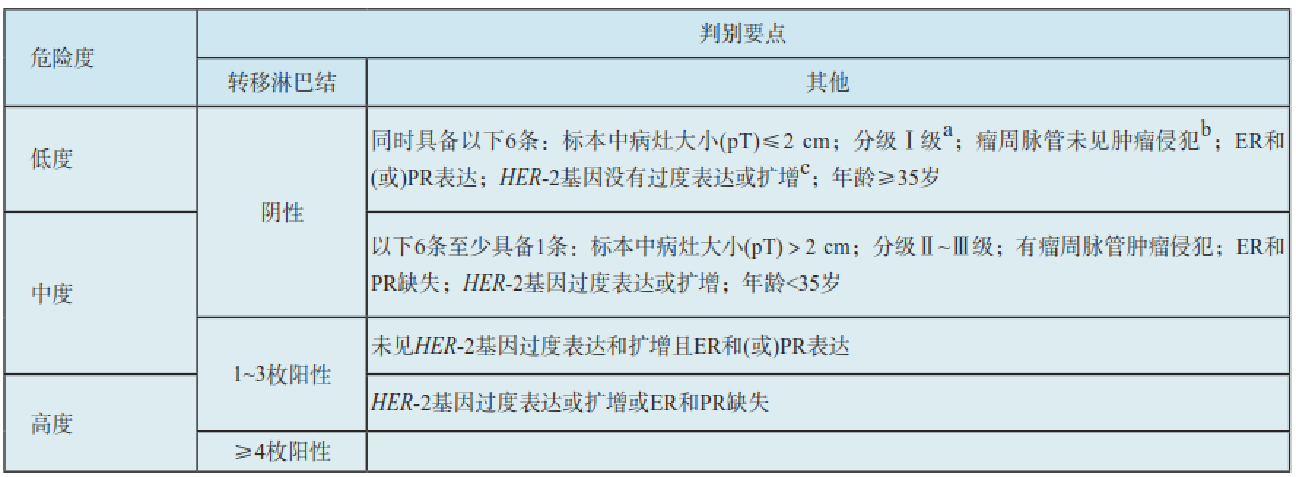
乳腺癌分子分型的標(biāo)志物監(jiān)測(cè)和判定
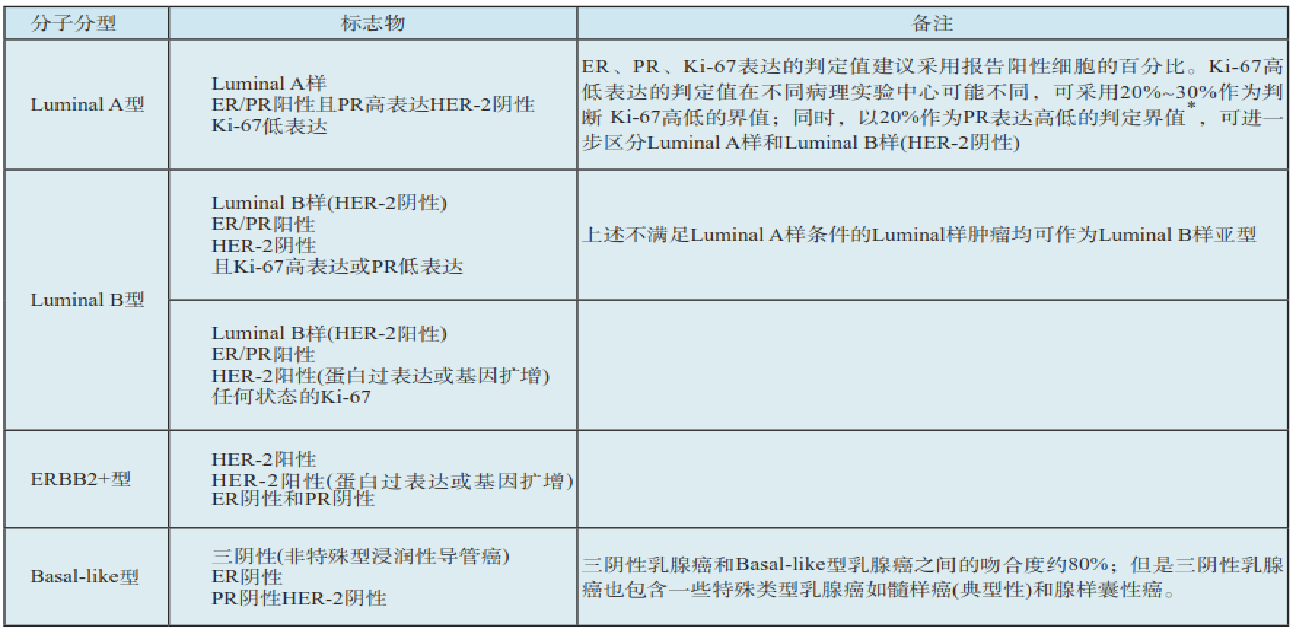
不同分子型的推薦治療

乳腺癌術(shù)后輔助化療適應(yīng)證:
⑴ 浸潤(rùn)性腫瘤大于2 cm。
⑵ 淋巴結(jié)陽(yáng)性。
⑶ 激素受體陰性。
⑷ HER-2陽(yáng)性(對(duì)T1a以下患者目前無(wú)明確證據(jù)推薦使用輔助化療)
⑸ 組織學(xué)分級(jí)為3級(jí)。
以上單個(gè)指標(biāo)并非化療的強(qiáng)制適應(yīng)證,輔 助化療方案的制定應(yīng)綜合考慮上述腫瘤的臨床病理學(xué)特征、患者生理?xiàng)l件和基礎(chǔ)疾患、患者 的意愿,以及化療可能獲益與由之帶來(lái)的不良 反應(yīng)等。免疫組織化學(xué)檢測(cè)應(yīng)該常規(guī)包括ER、 PR、HER-2和Ki-67。
禁忌證
⑴ 妊娠期:妊娠早、中期患者,應(yīng)慎重選擇化療。
⑵ 年老體弱且伴有嚴(yán)重內(nèi)臟器質(zhì)性病變患者。
注意事項(xiàng):
1、若無(wú)特殊情況,一般不建議減少化療的周期數(shù)。
2、在門(mén)診病歷和住院病史中應(yīng)當(dāng)記錄患者當(dāng)時(shí)的身高、體質(zhì)量及體表面積,并給出藥物的每平方米體表面積的劑量強(qiáng)度。一般推薦首次給藥劑量應(yīng)按推薦劑量使用,若有特殊情況需調(diào)整時(shí)不得低于推薦劑量的85%,后續(xù)給藥劑量應(yīng)根據(jù)患者的具體情況和初始治療后的不良反應(yīng),可以1次下調(diào)20%~25%。每個(gè)輔助化療方案僅允許劑量下調(diào)2次
3、輔助化療一般不與內(nèi)分泌治療或放療同時(shí)進(jìn)行,化療結(jié)束后再開(kāi)始內(nèi)分泌治療,放療與內(nèi)分泌治療可先后或同時(shí)進(jìn)行。
4、化療時(shí)應(yīng)注意化療藥物的給藥順序、輸注時(shí)間和劑量強(qiáng)度,嚴(yán)格按照藥品說(shuō)明和配伍 禁忌使用。
5、激素受體陰性的絕經(jīng)前患者,在輔助化療期間可考慮使用卵巢功能抑制藥物保護(hù)患者的卵巢功能。推薦化療前1~2周給藥,化療結(jié)束后2周給予最后1劑藥物。
6、蒽環(huán)類藥物有心臟毒性,使用時(shí)須評(píng)估LVEF,至少每3個(gè)月1次。如果患者使用蒽環(huán)類藥物期間發(fā)生有臨床癥狀的心臟毒性,或無(wú)癥狀但LVEF<45%亦或較基線下降幅度超過(guò)15%,可考慮檢測(cè)肌鈣蛋白,必要時(shí)應(yīng)先停藥并充分評(píng)估患者的心臟功能,后續(xù)治療應(yīng)慎重。
7、中國(guó)專家團(tuán)認(rèn)為三陰性乳腺癌的優(yōu)選化療方案是含紫杉和蒽環(huán)的劑量密度方案。大多數(shù)Luminal B(HER-2陰性)乳腺癌患者需要接受術(shù)后輔助化療,方案應(yīng)包含蒽環(huán)類和(或)紫杉類藥物。
乳腺癌術(shù)后輔助內(nèi)分泌治療:
適應(yīng)癥:激素受體ER和(或)PR陽(yáng)性的乳腺癌患者。
內(nèi)分泌治療與其他輔助治療的次序:輔助內(nèi)分泌治療與化療同時(shí)應(yīng)用可能會(huì)降低療效。一般在化療之后使用,但可以和放療及曲妥珠單抗治療同時(shí)應(yīng)用。
乳腺癌術(shù)后輔助曲妥珠單抗治療適應(yīng)癥:
原發(fā)浸潤(rùn)灶大于1.0 cm HER-2陽(yáng)性時(shí),推薦使用曲妥珠單抗;原發(fā)腫瘤在0.5~1.0 cm時(shí),可考慮使用。中國(guó)專家團(tuán)認(rèn)為對(duì)直徑不超過(guò)0.5 cm的浸潤(rùn)性HER-2陽(yáng)性腫瘤,曲妥珠單抗的選擇應(yīng)綜合考慮,如對(duì)于HER-2陽(yáng)性T1aN0乳腺癌,如果原發(fā)癌ER陰性且腫瘤大小接近 5 mm,可以考慮每周紫杉醇+曲妥珠單抗輔助治療;淋巴結(jié)微轉(zhuǎn)移的患者也應(yīng)考慮曲妥珠單抗治療。對(duì)于ER陽(yáng)性乳腺癌且腫瘤大小接近 1 mm的患者,當(dāng)估計(jì)復(fù)發(fā)風(fēng)險(xiǎn)小于5%且可以選擇內(nèi)分泌治療時(shí),輔助全身化療 抗HER-2的絕對(duì)獲益非常微弱。
相對(duì)禁忌證:
⑴ 治療前LVEF<50%。
⑵ 同期正在進(jìn)行蒽環(huán)類藥物化療。
放療的適應(yīng)證:
全乳切除術(shù)后,具有下列預(yù)后因素之一,則符合高危復(fù)發(fā),具有術(shù)后放療指征,該放療指征與全乳切除的具體術(shù)式無(wú)關(guān):
⑴ 原發(fā)腫瘤最大直徑大于等于5 cm,或腫瘤侵及乳腺皮膚、胸壁。
⑵ 腋窩淋巴結(jié)轉(zhuǎn)移大于等于4枚。
⑶ 淋巴結(jié)轉(zhuǎn)移1~3枚的T1-2,目前的資料也支持術(shù)后放療的價(jià)值,然而對(duì)低危亞組需權(quán)衡放療獲益和風(fēng)險(xiǎn)。術(shù)后放療可能在包含以下因素的患者中更有意義:年齡小于等于40歲,腋窩淋巴結(jié)清掃數(shù)目小于10枚時(shí)轉(zhuǎn)移比例大于20%,激素受體陰性,HER-2過(guò)表達(dá),組織學(xué)分級(jí)高,以及脈管陽(yáng)性等。
⑷ T1-2乳腺單純切除術(shù),如SLN陽(yáng)性,當(dāng)不考慮后續(xù)腋窩清掃時(shí),推薦術(shù)后放療;如不考慮放療,則推薦進(jìn)一步腋窩清掃。
乳腺癌的治療相對(duì)復(fù)雜,具體治療方案需在有經(jīng)驗(yàn)的醫(yī)療機(jī)構(gòu)制定個(gè)體化方案。
- 上一條:急性胰腺炎
- 下一條:什么是腹腔熱灌注化療
- 別再跟脂肪“死磕”了!外科減重:不是“切胃作弊”,而是給身體“重啟健康” 2025-11-30
- 乳腺包塊別慌:揭開(kāi)它的“真面目” 2025-10-31
- 你相信光嗎 2025-09-30
- 不容忽視的“腸道交通堵塞” 2025-08-31
- 小小闌尾,不可忽視-闌尾炎 2025-07-31











