宮頸癌篩查那些事兒
今天向大家介紹宮頸癌系列知識,目的是幫女性朋友選擇最適合自己的預防性篩查方法。我們先科普宮頸癌的發病原理,特別是病毒學方面的知識,進而介紹宮頸癌篩查的科學依據、篩查方法比較。病理報告如何解讀?也是大家關心的問題。篩查發現異常怎么辦?且聽在下娓娓道來。
一、宮頸癌的發病原理
宮頸癌的罪魁禍首是一種病毒,人乳頭瘤病毒,英文簡稱HPV。需要強調的是,HPV有很多亞型,其中能致癌的亞型稱為高危型HPV,包括:16,18,31,33,35,39,45,51,52,56,58,59,68。
那么,高危型HPV是怎樣導致宮頸癌呢?
從病毒學方面講,HPV病毒感染分為兩種階段。第一階段,稱為潛伏性感染。普通的方法檢測不到HPV病毒,宮頸細胞學篩查和病理學篩查都是陰性,只能用特殊的分子學檢查方法才能發現。第二階段是復制性病毒感染。HPV病毒在宮頸細胞內大量復制,導致棘層肥厚、細胞質空泡、挖空細胞、多核細胞和核異型性,普通的篩查方法能檢測到,如宮頸細胞學、宮頸活檢和HPV檢測。(圖1)
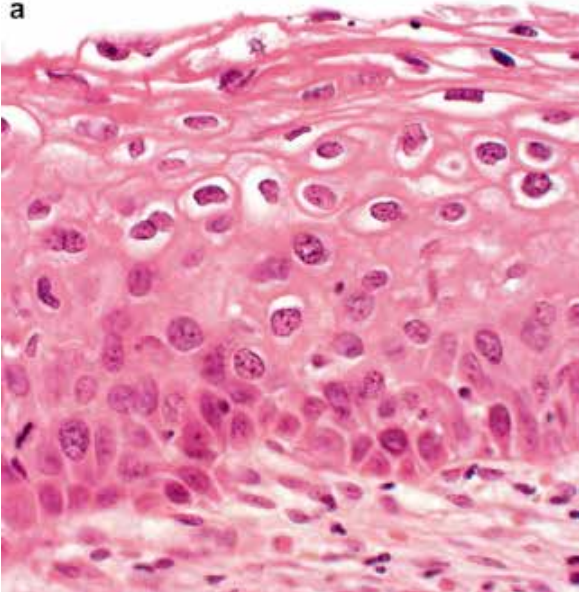
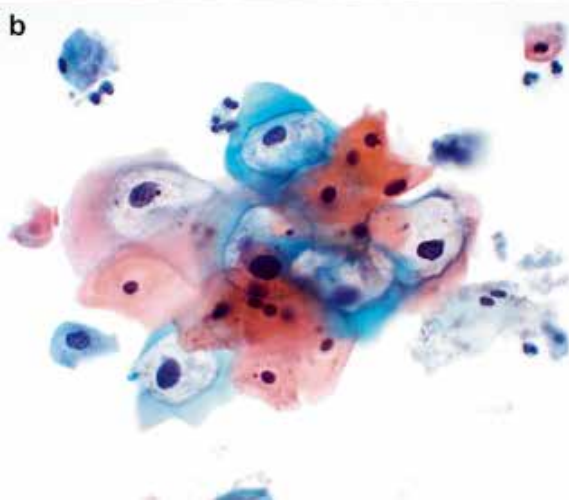
圖1.HPV感染導致的細胞病變。HPV感染導致的細胞病變包括核增大、核固縮或核深染、細胞大小不一、多核和核周胞質空泡化。a.典型的低度鱗狀上皮內病變(LSIL)的組織學特征;b.典型LSIL的細胞學特征
從流行病學方面講,HPV病毒感染都是接觸性傳播。在各種傳播方式中,性生活最常見,但并不是必然的感染途徑。估計每次性生活具有40%的傳播風險使用避孕套可減少但不能消除女性被傳染的風險。男性包皮環切術可減少HPV的攜帶與傳播。大多數女性在性生活開始后幾年內感染HPV。國外有一項研究,80%的女性大學生在某一段時間感染了HPV。
大多數HPV感染為暫時性的,且病毒會被清除或潛伏1到2年。如果感染持續存在36個月以上,那么病毒在將來被清除的可能性顯著降低。而且,感染持續時間越長,進展為高級別病變的可能性越高。在細胞學正常的20歲左右的女性中,高危型HPV的陽性率比較高,并且隨著年齡的增長而下降。
二、宮頸癌篩查的科學依據
從感染高危型HPV到發生宮頸癌,是一個漫長的過程,并且這個過程是可以檢測的、可以治愈的,這就是宮頸癌篩查的科學依據。
國內外多種學術機構都制定了科學的篩查指南,可以簡單地歸納為針對病毒的篩查(HPV檢測)、針對細胞的篩查(宮頸細胞學篩查,如TCT)和聯合篩查(HPV TCT)這三大類篩查方法。最新指南強調了HPV檢測用于初篩的價值,同時基于“同等風險,同等管理”的理念,在HPV初篩陽性的管理中,HPV16/18型具有最高的風險,需要直接轉診陰道鏡,而其他12種亞型陽性,通過細胞學或者醋酸染色目視觀察(VIA)進行分流。
三、宮頸癌篩查:方法比較
HPV檢測:主要檢測高危型HPV。優點:自動化檢測,靈敏度高。缺點:存在假陽性;病毒感染并不一定致病,HPV檢測用于大規模篩查會導致社會資源的浪費。
TCT檢測:檢測宮頸細胞。如前所述,復制性病毒感染才會導致細胞學異常,所以避免了HPV檢測的假陽性和雖然HPV陽性但不致病的那些人群,節省社會資源,減少不必要的恐慌。這是其優點,但也有缺點,需要經過培訓的、有經驗的病理醫生,人力成本高,工作量有限,存在漏診的可能性。
聯合篩查:同時檢測HPV和細胞學。優點是這種篩查方法彌補了各自單獨篩查的缺點,具有高度敏感性和高度特異性。缺點是成本高,不適合大規模篩查。
四、陰道鏡活檢--宮頸鱗狀上皮內病變的病理報告解讀
篩查發現異常,醫生會根據行業規范或指南,可能會建議做陰道鏡檢查和宮頸活檢。“活檢”是一種病理檢查方法,是疾病診斷的金標準。活檢發現異常,后續可能會做宮頸錐形切除手術,并進一步做病理檢查,這部分內容已經超出本次科普的范圍,容我后續詳述。宮頸宮頸錐形切除和/或其他宮頸手術后,仍然需要定期做宮頸癌篩查。
1、定義
宮頸的鱗狀上皮內病變(SIL),也稱為宮頸上皮內瘤變(CIN),是由HPV感染驅動的鱗狀細胞增殖,顯示成熟異常和/或病毒性細胞學改變,未突破基底膜。它們分為低度鱗狀上皮內病變(LSIL)和高度鱗狀上皮內病變(HSIL)。
2、正常鱗狀上皮
子宮頸成熟鱗狀上皮從基底層向上逐漸成熟,中層細胞空泡化,基底細胞為單層,核垂直于基底膜。在上皮間質連接處,可見指狀纖維血管間質乳頭突入上皮下部。(圖2)
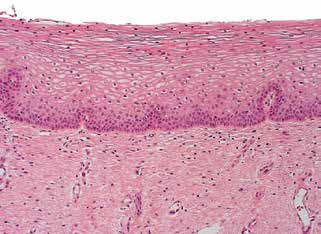
圖2.正常鱗狀上皮
3、低度鱗狀上皮內病變(LSIL)
LSIL的特征是基底層細胞/副基底層細胞在上皮的下1/3層增殖,可顯示核分裂活性,但沒有非典型核分裂象,并且可有挖空細胞異型性伴成熟/分化的特征。(圖3)
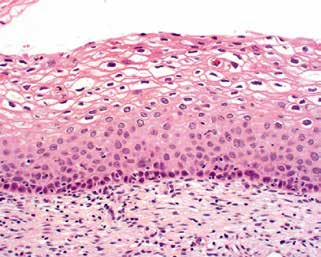
圖3.低度鱗狀上皮內病變(LSIL)的上皮下1/3層僅有輕微的細胞異型性
4、高度上皮內瘤變
在HSIL中,非典型性應當見于鱗狀上皮全層,其范圍和程度均超過LSIL。基底層和副基底層具有顯著的核非典型性和AMF。不成熟基底型細胞占據上皮的下1/3層以上。
4.1 HSIL(CIN 2)
不成熟基底樣細胞占上皮厚度的2/3,但未累及上1/3。同樣,核分裂象只出現在上皮的下2/3層,而不出現于上1/3層。(圖4)
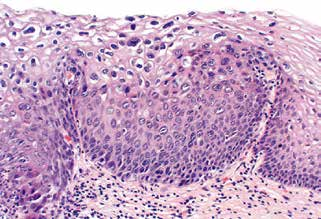
圖4.HSIL伴明顯的挖空細胞病。除了不成熟基底樣細胞延伸至上皮中層之外,該病變還有挖空細胞病的特征。這種病變以前被歸類為CIN2
4.2 HSIL(CIN 3)
不成熟基底樣細胞累及上皮層的上 1/3,核分裂象可見于上皮全層(圖5)。
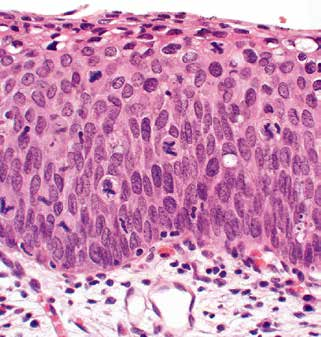
圖5.HSIL。這種HSIL的不成熟基底樣細胞和核分裂象幾乎延伸至上皮表面。該病變以前被歸類為CIN3
5、實際病例
如下圖,你認為這個病例是LSIL還是HSIL?
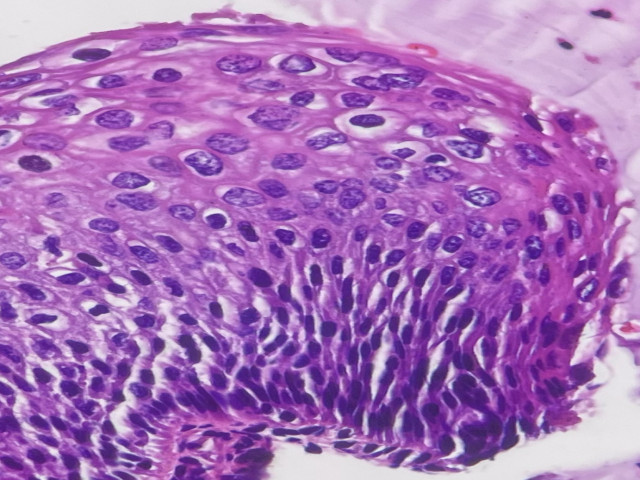
分析:全層鱗狀細胞都有顯著的異型性,所以是高度病變(HSIL)。
不成熟基底型細胞占據上皮的下1/3層以上,但未到達下2/3層,大概到達1/2層,所以是CIN2。
垂直排列的小細胞都是不成熟基底型細胞。
附臨床信息:女,36歲,常規篩查發現異常(HPV16 ,TCT HSIL),行陰道鏡活檢。免疫組化:p16
進一步圖解如下:
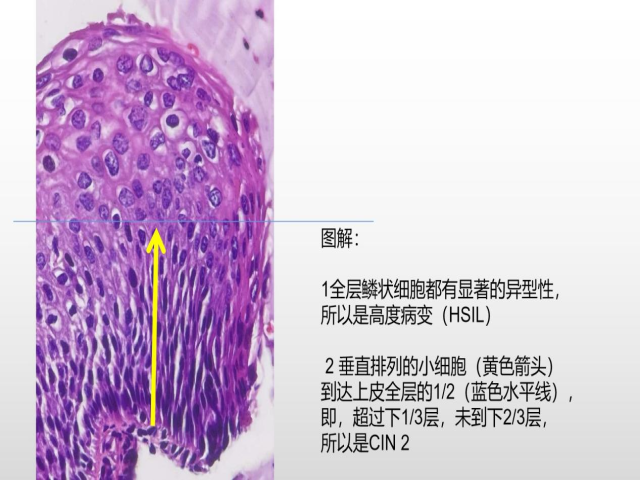
五、篩查建議
以下摘錄2021年版世界衛生組織(WHO)宮頸癌篩查指南中“對一般女性的具體篩查建議”,供大家參考。國內也有相似的指南,有興趣者可自行在網上查閱。
一般女性無論選擇哪種策略,均建議:從30歲起進行HPV檢測,每5-10年定期篩查一次。關于篩查方法、頻率及相關處理,具體推薦和管理規范聲明如下:
1、建議在篩查和治療方法中使用HPV檢測作為主要篩查方法。
2、無論是否采用分診策略,HPV檢測均是首選初步篩查方法。
3、在“篩查和治療”策略中,建議對HPV檢測呈陽性的女性進行治療。在“篩查、分診和治療”策略中,對HPV檢測呈陽性的女性,建議通過基因分型、陰道鏡檢查、VIA或細胞學檢查進行分診。
4、進行HPV檢測時,建議由醫療衛生專業人員采樣或由女性自行采樣。自行采樣可能讓患者更自在,但需得到專業指導。
5、一般女性從30歲開始定期進行宮頸癌篩查。
6.50歲以后,如按WHO建議的篩查間隔定期篩查且連續兩次均為陰性,則可停止篩查。
7、應優先篩查30-49歲的一般女性。當有適合的診療方法時,還應優先考慮50-65歲女性年齡段從未接受過篩查的女性(管理規范聲明)。
8、如以HPV檢測作為主要篩查方法,每隔5-10年定期篩查。
9、如果HPV檢測尚未實施,仍使用VIA或細胞學作為主要篩查方法,則需每3年定期篩查。
10、即使一生只進行兩次篩查,也是有益的(管理規范聲明)。
11、如初步篩查為HPV檢查,呈陽性,但在后續分診檢測中呈陰性,則24個月后重新進行HPV檢測,如果陰性,則可轉為常規定期篩查間隔。
12、如初步篩查為細胞學呈陽性,但陰道鏡檢查結果正常,則12個月時重新進行HPV檢測,如果陰性,則可轉為常規定期篩查間隔。
13、因組織學證實的CIN2/3或原位腺癌(AIS)或因陽性篩查結果而已經接受治療,在12個月時優先重新進行HPV檢測,如果陰性,則可轉為常規定期篩查間隔。
14、在引入HPV檢測的機構,無論女性既往篩查采用的是什么方法,下一次常規篩查都使用HPV檢測。如目前篩查仍以細胞學或VIA檢查為主,則繼續使用,直至HPV檢測可用(管理規范聲明)。
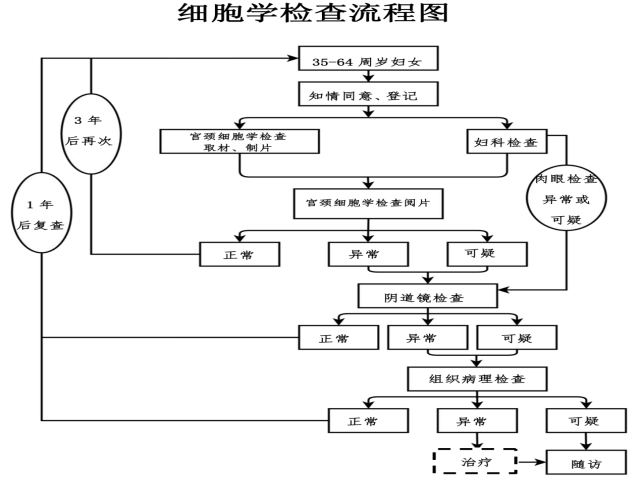
附1:國家衛生健康委印發《宮頸癌篩查工作方案》2021年版細胞學檢查流程圖
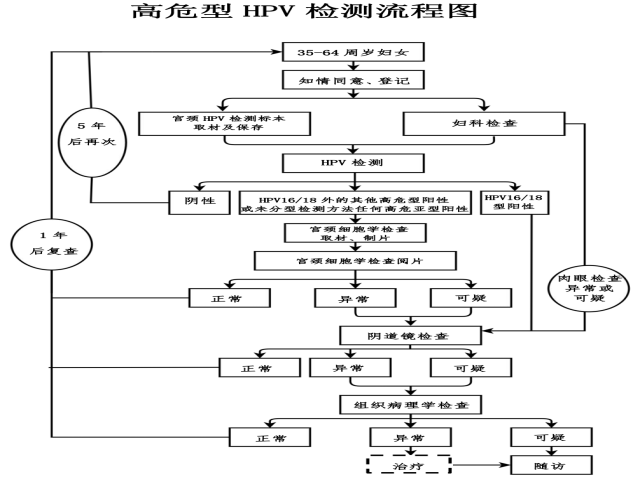
附2:國家衛生健康委印發《宮頸癌篩查工作方案》2021年版HPV檢測流程圖
文章轉自華夏病理網
- 胎盤絨毛毛細血管增生病變(二) 2024-09-27
- 胎盤絨毛毛細血管增生病變(一) 2024-08-30
- 肺腺癌為什么越來越多女性發生 2024-06-21
- 基底細胞癌 2024-02-28
- 毛母細胞瘤 2023-11-29











